
超数排卵:小鼠模型中的时间密码
在辅助生殖与发育生物学研究中,超数排卵(superovulation)是获取高质量卵母细胞的关键技术。小鼠超数排卵推荐每只雌鼠注射PMSG 5-10 IU,48 h后注射HCG 5-10 IU,在注射HCG后14-16 h进行受精[1]。然而,PMSG与HCG的“48小时定律”背后,隐藏着卵泡同步化与卵母细胞成熟的精密时钟。
小鼠自然发情仅释放10–15枚卵子。通过外源激素干预,可突破这一限制:首先PMSG(孕马血清促性腺激素)模拟FSH效应,同步募集并激活大量原始卵泡,使其发育至有腔阶段,此时的卵母细胞仍停滞于第一次减数分裂双线期(GV期);间隔48 h后给予HCG(人绒毛膜促性腺激素),模拟LH峰,诱导GV期卵母细胞恢复减数分裂,排出第一极体并停滞于第二次减数分裂中期(MII)。最终,在输卵管壶腹部聚集大量同质化的MII期卵子,为体外受精和后续胚胎操作提供充足且高质量的材料。
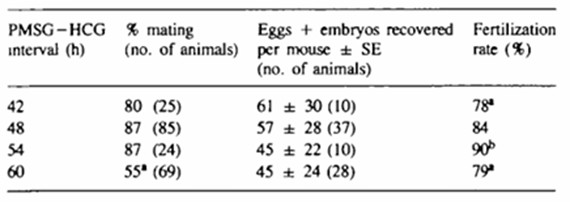
PMSG通过模拟FSH,需44-48小时募集足够数量的小卵泡并使其同步发育至排卵前阶段。George[2]研究发现,将PMSG-HCG间隔从48小时延长至60小时,并未提升小鼠见栓率与受精率(Table 1.);与此同时,延长注射时间也未能协助胚胎克服2-细胞阻滞(Table 2.)。这一结果提示,48小时可能是卵泡群同步化与卵母细胞核成熟的“黄金窗口”。

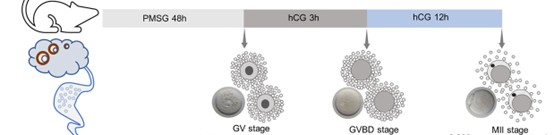
注射HCG模拟LH峰后,卵母细胞恢复减数分裂,经历生发泡破裂(GVBD),最终在12-14小时内完成第一次减数分裂并排出第一极体,达到MII,此时方具备受精能力(Figure 1.)。取卵时机必须精准契合此成熟窗口:过早取卵(如HCG后<12小时)可能获得大量停滞在GV期或MI期的未成熟卵母细胞,无法受精;而过晚取卵(如HCG后>16小时),卵母细胞则开始进入老化阶段,表现为皮质颗粒提前释放、纺锤体结构异常等,从而导致受精率下降或胚胎发育潜能受损。因此,HCG后14-16小时是获取成熟MII期卵母细胞并进行受精的理想时间窗。
• 激素保存:PMSG与HCG均为糖蛋白,反复冻融会导致空间结构变性。建议单次分装-20℃保存,避免活性损失。
• 取卵时机:HCG注射后14-16小时后取卵,可最大化获取输卵管壶腹部成熟卵母细胞。
George等的数据警示我们:在超数排卵方案中,时间间隔并非“越长越好”。延长激素间隔可能扰乱卵泡微环境,最终损害胚胎基因组激活。未来需结合单卵母细胞转录组与实时成像技术,解析48小时定律的分子计时器。48小时,是进化赋予小鼠的生殖节拍器;14-16小时,是卵母细胞等待精子的终极倒计时。精准把握每一小时,才能让每一次超排成为“质量”而非“数量”的胜利。